Tema 6 - Farmacocinetica: Metabolismo - 17/09-1/09
Clase del 17/09 dada por Laura
Presentación

La biotransformación es el conjunto de transformaciones químicas que sufre un fármaco dentro del organismo, catalizadas por enzimas, para hacerlo más hidrosoluble y fácil de eliminar.
Para metabolizarlo se busca hacerlo menos liposoluble y mas lo ionizado, lo contrario que en distribución.
Los sitios de biotransformación son:
- Higado
- Tubo digestivo (Jugo gastrico, enzimas digestivas, flora intestinal)
- Sangre (hidrolasas y enterasas)
- Riñon
- Placenta
- SN central y periferico
Fases del metabolismo:
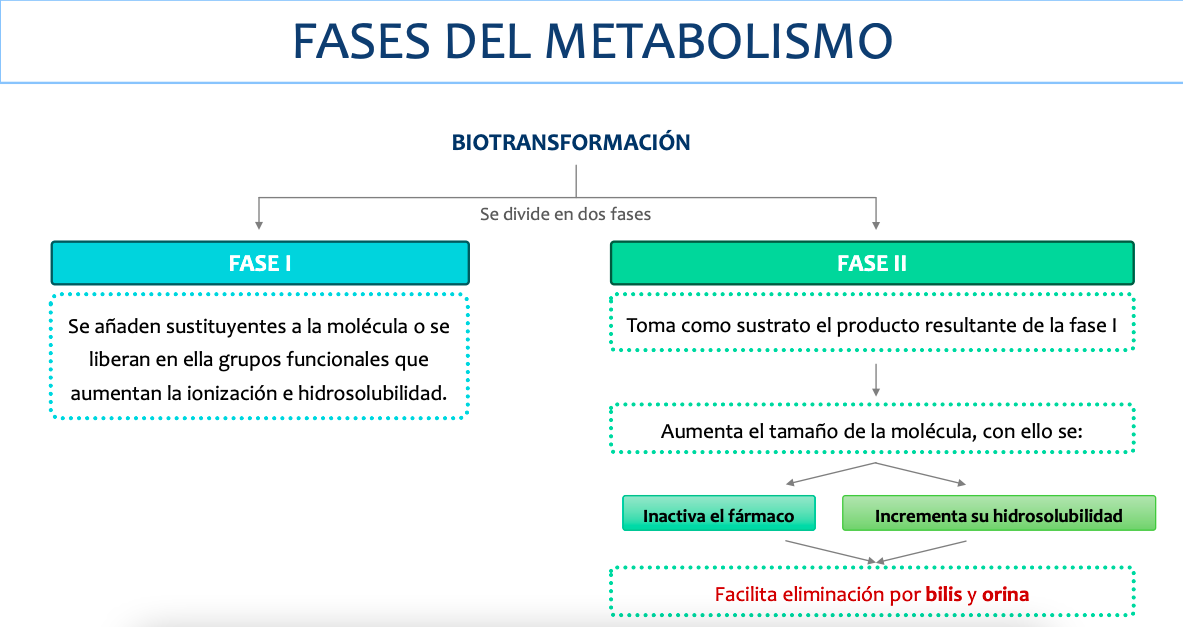
Dos fases, 1 en la que se añaden sustituyentes para añadir hidrosolubiliadad e ionización. en la 2 se toma el resultado de la fase 1 y se aumenta el tamaño para inactivarlo y solubilizarlo para su posterior eliminacion por bilis y orina.
Fase 1: Reacciones de funcionalización
- Adición de grupos funcionales: -OH, -COOH, -NH2, -SH2
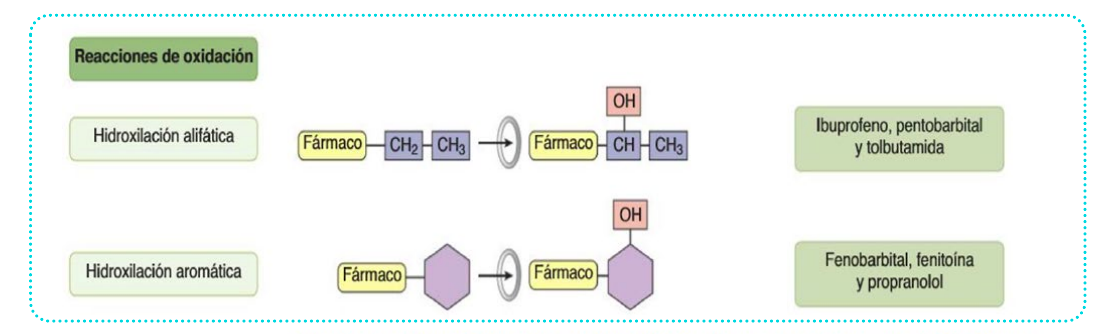
- Oxidación: Por los citocromo P450 del higado (sistema de oxidación microsomal, en el reticulo citoplasmatico liso) requiere energia para realizarse LA MAS IMPORTANTE
Hay oxidación no microsomal pero es menos importante, se realiza en citosol y mitocondrias
Clase del 18/09 dada por Laura
Fase I: reacciones de funcionalización
Menos importantes.
Son importantes porque si el fármaco no tiene esos grupos funcionales, no pueden seguir las reacciones de fase 2 donde se conjugan.
Azorreducción
Nitroreducción (Ej.: nitroreducción por flora intestinal).
Se pueden producir a nivel hepático por el sistema enzimático microsomal o a nivel intestinal por la flora bacteriana.
La Oxidación y Reducción alteran o crean nuevos grupos funcionales.

Normalmente en sangre
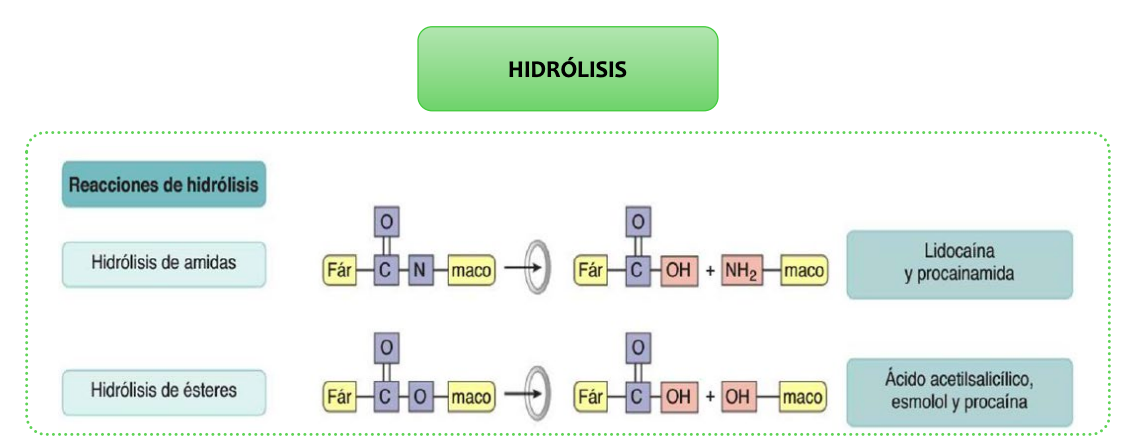
Varios tipos: Hidrólisis de ésteres (esterasasas) y amidas (amidasas) oHidrólisis de enlaces peptídicos (peptidasas)
La hidrólisis rompe los enlaces ésteres, amidas y peptídicos liberando nuevos grupos funcionales.
Las enzimas se encuentran en plasma, hematíes , sistema microsomal hepático y otros tejidos
En la fase 1 las reacciones de funcionalización sirven para producir un aumento en la polaridad de la molecula.
Se puede inactivar el farmaco
Hay medicamentos que tienen el farmaco inactivado. Al metabolizar un farmaco inactivado lo convierten en un profarmaco o un farmaco activado.
Convierte un producto activo en otro activo (formación de metabolitos activos o tóxicos).
Fase II: reacciones de conjugación
El objetivo es aumentar polaridad mediante unión con moléculas endógenas (requiere energía).
Se producen cuando el fármaco o metabolito de primera fase contiene un grupo químico como hidroxilo (-OH), carboxilo (- COOH), amino (-NH2) o sulfhidrilo (-SH2) apropiado para combinarse con moléculas de origen endógeno como ac. glucurónico, grupos sulfato, acetilo, metilo, formando metabolitos polares hidrosolubles e inactivos fácilmente eliminables.
5 tipos de conjugación
Conjugación con ácido glucurónico
Conjugación con sulfato
Acetilación
Metilación
Conjugación con aminoácidos
Conjugación con acido glucoronico
TODOS LOS ACIDOS PARA PODER SER CONJUGADOS CON ACIDO GLUCURONICO DEBEN DE TENER GRUPOS OH, NH, COOH Y SH
Fracción soluble del hígado: síntesis de ácido uridindifosfato glucurónico (UDPGA) a partir de glucosa.
UDPGA: donador de ácido glucurónico para conjugar fármacos/metabolitos.
Enzimas: UDP-glucuroniltransferasa en microsomas hepáticos.
Fármacos/metabolitos deben tener grupos: -OH, -NH₂, -COOH, -SH₂.
Gran capacidad de glucuronidación por múltiples formas enzimáticas.
Gato: deficiencia en glucuronidación → riesgo de acumulación y toxicidad.
El acido acetil salicilico o aspirina es uno de estos. Por eso no es recomendable en gatos, lo pueden metabolizar pero muy mal. Solo en casos especificos, tarda mucho en eliminarse.
Conjugación con sulfato:
Conjugación importante para grupos fenólicos y grupos -OH alifáticos.
Ocurre en la fracción soluble del hepatocito.
Requiere activación previa del grupo sulfato.
Enzimas: sulfotransferasas.
Especie deficitaria: cerdo.
Acetilación
Incorporación de radical acetilo (acetil-CoA) a grupos amino o carboxilo.
Enzimas: acetiltransferasas.
Reacción en la fracción soluble del hepatocito.
Ejemplo: sulfamidas → metabolitos por acetilación.
Especie deficitaria: perro.
Metilación
Conjugación de un grupo metilo (de metionina).
Se une a grupos -OH, -SH o -NH₂ del fármaco/metabolito.
Enzimas: metiltransferasas.
Localización: fracción soluble del hepatocito.
Conjugación con aminoacidos:
Conjugación con aminoácidos (glicina, ornitina, etc.).
Enzimas localizadas en mitocondrias.
Se unen a grupos -COOH del fármaco/metabolito.
Factores que modifican el metabolismo:
Factores Fisiologicos: Edad, especie, hormonal, genetico, nutritivo
Factores patologicos: Hepatopatias, enfermedades hereditarias (siameses y collies tienen diferentes enzimas)
Farmacologicos: Inducción enzimatica o inhibición enzimatica
Metabolismo de productos toxicos:
Paracetamol o Acetaminofenol: se metaboliza en el higado mediante glucorización y sulfatación y se eliminan los metabolitos no toxicos. A dosis terapeuticas con el Citocromo P450 el NAPQI que es un metabolito muy toxicos se inactiva por el glutation pero a dosis superiores se acaba el glutation y se podrucen daños en el higado.
En gatos ni la sulfatación ni la glutación la funcionan bien, el paracetamol es super peligroso, mortal, la aspirina o acido salicilico es peligroso pero se le puede dar porque no produce metabolitos toxicos, el paracetamol si lo crea.
Para revertir los efectos del paracetamol, se añade glutation en forma de N-acetilcisteina para que neutralice el NAPQI resultante de la oxidación del paracetamol